Синтез мРНК
мРНК становятся удобным и очень эффективным средством доставки генетической информации в клетки. Разработка мРНК-вакцин и мРНК-терапии является одной из самых приоритетных задач в лабораториях всего мира!
С помощью синтезированных мРНК можно решить множество научных задач: экспрессия репортерных белков, доставка систем геномного редактирования, временная экспрессия гена-мишени, оценка эффективности новых систем доставки.
С помощью синтезированных мРНК можно решить множество научных задач: экспрессия репортерных белков, доставка систем геномного редактирования, временная экспрессия гена-мишени, оценка эффективности новых систем доставки.
1
Введение
Транскрипция in vitro — это процесс получения молекул РНК на матрице ДНК за пределами живой клетки «в пробирке». Использование данного метода позволяет создавать специфические последовательности РНК для различных целей, таких как изучение экспрессии генов и получение РНК для функциональных или структурных исследований. С помощью проведения транскрипции in vitro можно нарабатывать различные виды РНК, включая короткие регуляторные и направляющие РНК для систем геномного редактирования. В настоящий момент наблюдается особый интерес к получению искусственных матричных РНК (мРНК), с помощью которых можно решить множество научных задач: экспрессия репортерных белков, доставка систем геномного редактирования, временная экспрессия гена-мишени, оценка эффективности новых систем доставки.
Для обеспечения наработки функциональной молекулы мРНК необходимо учитывать целый ряд ее структурно-функциональных особенностей (Рис.1). Ключевая задача при синтезе – создать молекулу мРНК, структура которой будет имитировать ее созревание внутри клеток. С 5’-конца в эукариотических мРНК находится КЭП – особый модифицированный нуклеотид, обеспечивающий защиту транскрипта от деградации под действием экзонуклеаз. С 3’-конца молекулу защищает длинная цепь из остатков аденозинмонофосфата (поли(А)-хвост). 5'-кэп и полиА-хвост обеспечивают успешную посадку рибосомы для эффективной инициации трансляции с матрицы мРНК. Кодирующая область мРНК обычно с двух сторон фланкирована структурированными нетранслируемыми регионами, которые регулируют трансляционную активность и стабильность мРНК. Кроме того, особую роль в обеспечении длительной функциональной активности и стабильности мРНК выполняют различные модифицированные нуклеотиды, которые формируются специальными ферментами в кодирующей и в нетранслируемых областях молекулы. Наиболее полную картину модификаций в мРНК и длинных некодирующих РНК можно изучить по результатам исследований, собранных в базах данных, например, RMBase v3.0, так как этому направлению даже дали отдельное название «эпитранскриптомика». Хотя роль отдельных модификаций вызывает по-прежнему живой научный интерес и пока до конца не изучена, ученые уже придумали, как использовать такие модификации для улучшения свойств искусственных РНК.
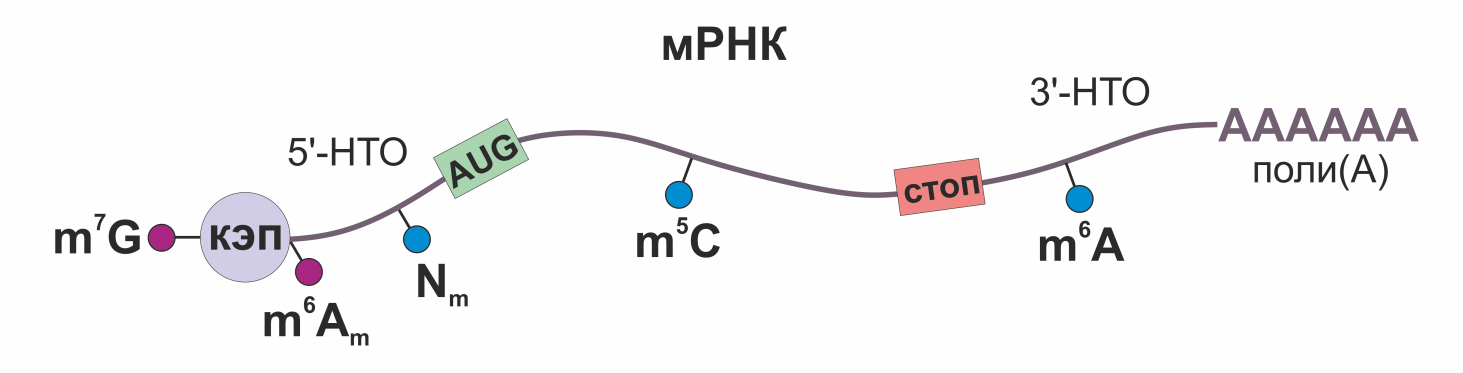
Рис.1 Структура мРНК
2
Подготовка к проведению синтеза мРНК
Конечно, в самом начале нужно сказать, что работа с РНК требует особой аккуратности: нужно обязательно использовать перчатки и халаты, проводить эксперименты в специально отведенных «чистых» местах, так как любые загрязнения и сами операторы работы являются активным источником нуклеаз, которые быстро разрушают РНК. В комнате, в которой планируется синтез РНК нельзя работать с препаратами РНКаз, даже в низких концентрациях! Все растворы для работы с РНК должны быть приготовлены на воде, обработанной DEPC. Мы рекомендуем использовать для растворения и разбавления растворов РНК специально подготовленную воду SP010-05, которую можно найти в разделе «Отдельные компоненты для ПЦР»
Синтез мРНК начинается с подготовки матрицы для транскрипции. Обычно, в качестве ДНК-матрицы выступает линеаризованная плазмида или фрагмент ДНК, полученный методом ПЦР, который содержит целевой ген или иную заданную последовательность (Рис.2). Для создания заданных конструкций рекомендуем использование Фьюжн ДНК-полимеразы и Т4-ДНК-лигазы от компании «Биолабмикс» (E-2050). Для выделения и очистки плазмидной ДНК рекомендуем использование набора от компании «Биолабмикс» (Plasmid-250-mini или Plasmid-20-maxi). В случае использования плазмиды в качестве матрицы, ДНК должна быть линеаризована по сайту, который ограничивает длину матрицы и обеспечивает остановку полимеразы в нужном положении. Кроме того, рекомендуем очищать ДНК–матрицу перед постановкой реакции транскрипции с использованием набора DR.
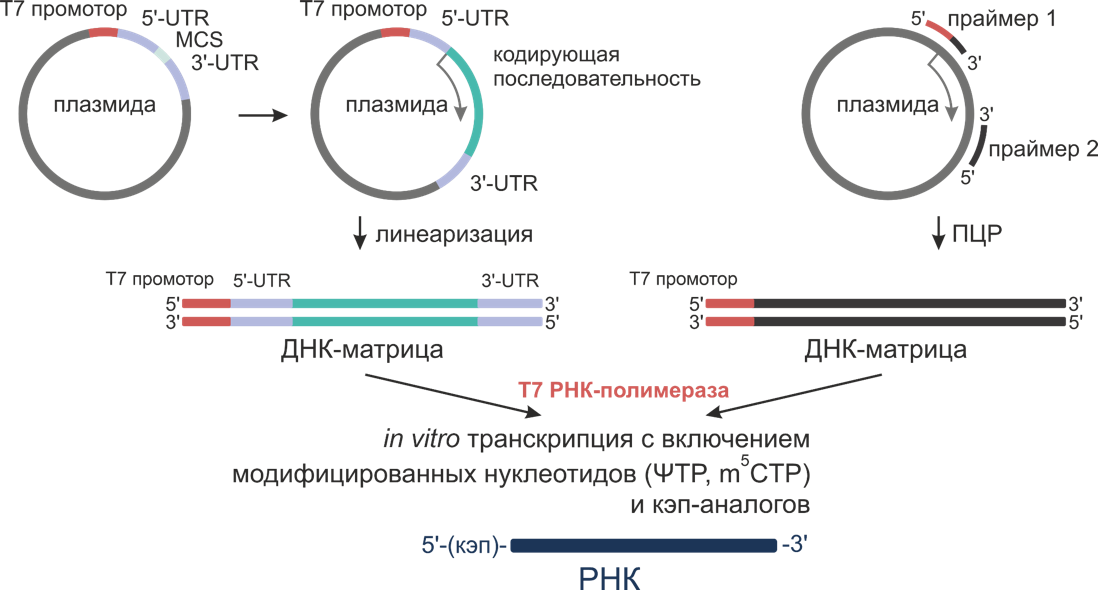
Рис. 2 Процесс подготовки ДНК-матрицы для транскрипции
Если в качестве матрицы планируете использовать ПЦР-фрагмент, то ПЦР с целевого участка геномной, вирусной или плазмидной ДНК рекомендуем проводить только с использованием высокоточной полимеразы. Это необходимо для того, чтобы предотвратить возникновение нуклеотидных замен в матрице, которые могут привести к нарушению функциональной активности синтезированной мРНК. Для получения длинных продуктов ПЦР нужно использовать высокоточную Фьюжн ДНК-полимеразу (Pfu-Sso7d) из каталога компании «Биолабмикс». Если необходимо подобрать условия амплификации, то удобнее будет использовать набор для проведения ПЦР с Фьюжн ДНК-полимеразой (KH041-500).
Важно!
В процессе подготовки матрицы также необходимо учитывать несколько важных аспектов. Во-первых, она должна содержать промоторную последовательность, распознаваемую РНК-полимеразой. Например, в случае использования ДНК-зависимой РНК-полимеразы Т7 от компании «Биолабмикс» (E-1010), матрица, соответственно, должна содержать T7 промотор. Во-вторых, необходимо корректировать последовательность следующую за промотором в зависимости от варианта аналога кэпа, используемого в эксперименте.
В настоящий момент в каталоге компании «Биолабмикс» представлено два варианта:
Аналог кэпа m7GmAmG (AGME-0050) или m7(3’OMeG)ppp(2’OMeA)pG – требуемая последовательность за промотором начинается с нуклеотидов AG (подробная инструкция представлена в описании готовых наборов для синтеза cap1-кэпированных мРНК www.biolabmix.ru/catalog/rna-transcription-mrna/transcription-kits/).
Для более хорошо известного аналога кэпа ARCA (ARCA-0050) – требуемая последовательность за промотором начинается с гуанозина, иными словами, первое основание, включаемое в РНК: G; следующие NN: оптимально CG (подробная инструкция представлена в описании готовых наборов для синтеза ARCA-кэпированных мРНК www.biolabmix.ru/catalog/rna-transcription-mrna/transcription-kits/).
Оба кэпа ARCA и m7(3’OMeG)ppp(2’OMeA)pG сконструированы таким образом, чтобы предотвращать возможную встройку в противоположной ориентации за счет наличия 3’-O-метильной группы в составе m7G. Кэп m7(3’OMeG)ppp(2’OMeA)pG обеспечивает более высокую эффективность кэпирования и не ингибирует реакцию транскрипции, что позволяет получать закономерно более высокие выходы при синтезе мРНК (Рис.3). Благодаря наличию 2’-O-метильной группы в составе первого нуклеотида применение m7(3’OMeG)ppp(2’OMeA)pG позволяет получить cap1-кэпированную РНК, которая более эффективно транслируется в клетках млекопитающих.
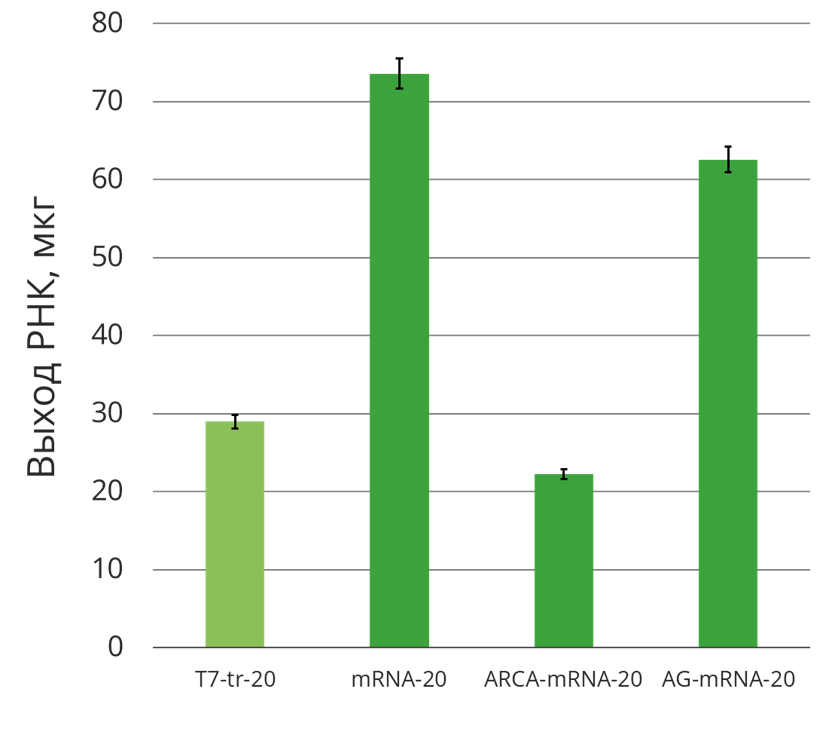
Рис. 3 Эффективность различных наборов для синтеза мРНК
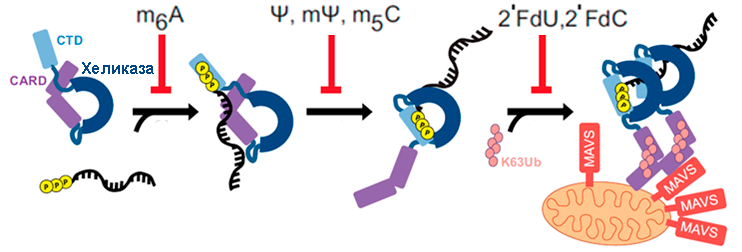
Рис. 4 Молекулярные механизмы, демонстрирующие вовлеченность модифицированных нуклеотидов в процесс предотвращения активация иммунного ответа
Благодаря работам Нобелевских лауреатов Каталин Карико и Дрю Вайсмана, а также ряда других исследовательских групп в настоящее время хорошо известно, что модифицированные нуклеотиды значительно улучшают свойства искусственных РНК: снижают цитотоксическую активность и подавляют активацию неспецифического иммунного ответа. В клетках млекопитающих экспрессируется целый ряд РНК-рецепторов, которые настроены на детекцию чужеродной РНК. Эти механизмы были созданы и отобраны эволюционно для защиты от заражения вирусами, несущими свой генетический материал в виде РНК. Так, на появление не модифицированной и некэпированной РНК в клетках реагируют Toll-like рецепторы, RIG-I, PKR, белки семейства IFIT. Связывание этих белков с РНК запускает каскады клеточного врожденного иммунного ответа и процессы, направленные на деградацию РНК и остановку трансляции в клетках. На уровне организма появление немодифицированных РНК приводит к выработке цитокинов и воспалительным процессам, которые становятся токсичными. В цикле работ, первые из которых были опубликованы еще в 2005 году, было показано, что включение в состав искусственных РНК модифицированных нуклеотидов, таких как псевдоуридин (Ψ), 5-метилцитидин (m5C), N1-метил-псевдоуридин (m1Ψ) и N6-метиладенозин (m6A), позволяет «обмануть» РНК-рецепторы и предотвратить активацию нежелательных процессов. Сейчас уже описаны подробные молекулярные механизмы, демонстрирующие, что одни модифицированные нуклеотиды препятствуют связыванию РНК с РНК-рецепторами, другие нарушают, конформационные перестройки РНК-белковых комплексов, которые необходимы для передачи сигнала от РНК-рецептора далее на эффекторные молекулы (Рис.4).
Стоит отметить, что стратегию с включением модифицированных природных нуклеотидов используют не только для синтеза мРНК, но и для получения других функциональных РНК, например, коротких регуляторных и РНК для систем CRISPR/Cas.
Портфолио для синтеза РНК компании Биолабмикс содержит весь перечень необходимых модифицированных NTPs для получения функциональных мРНК (Рис.5).
Рис 5. Модифицированные нуклеотиды: (1) N6-метиладенозин-5`-трифосфат (TNA-0050, Биолабмикс); (2) 5-метилцитидин-5'-трифосфат (TMC-0050, Биолабмикс); (3) Псевдоуридин-5'-трифосфат (TPU-0050, Биолабмикс); (4) N1-метил-псевдоуридин-5`-трифосфат (TNP-0050, Биолабмикс)
3
Транскрипция in vitro
Основой синтеза целевой молекулы мРНК является реакция транскрипции in vitro. Для ее проведения необходимо собрать все необходимые компоненты: матрицу, РНК-полимеразу (Т7) (E-1010), смесь рибонуклеозидтрифосфатов (rNS-410) (Рис. 6). После чего полученную смесь необходимо инкубировать при температуре 37°C
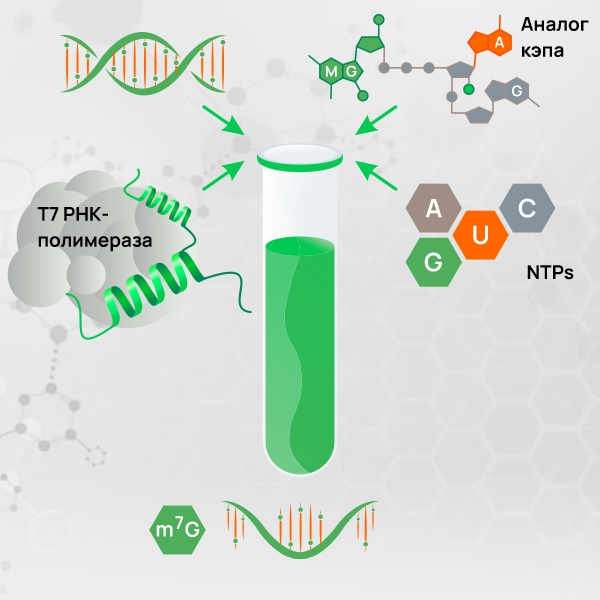
Рис. 6. Основные компоненты для синтеза мРНК
Для обеспечения стабильности РНК в растворе, в реакцию может быть добавлен ингибитор РНКаз. Рекомендуем использовать ингибитор РНКаз от компании «Биолабмикс» (RI-0020)
В зависимости от последовательности и конечного применения синтезируемой мРНК индивидуальная оптимизация отдельных этапов протокола может улучшить как выход реакции, так и биологическую функцию мРНК. Из литературы хорошо известно, что в состав мРНК можно включить модифицированные нуклеотиды, такие как N1-метил-псевдоуридин (m1Ψ), 5-метилцитидин (m5C), псевдоуридин (Ψ) и N6-метиладенозин (m6A) в разных соотношениях.
К вариабельным параметрам реакции можно отнести изменение времени инкубации или изменение количества ДНК–матрицы. Кроме того, при работе с короткими ДНК–матрицами (< 0.5 т.п.н.) рекомендуется увеличить время инкубации до 4-х часов. Можно инкубировать реакцию при 37°С в течение 16-18 часов (ночь).
Для достижения наилучшего результата рекомендуем использование наборов от компании «Биолабмикс», в которых уже собраны все необходимые компоненты, а также подобраны оптимальные условия для проведения реакции:
Набор для синтеза мРНК in vitro (с ΨTP и m5CTP с m7GmAmG) (AG-mRNA-YC-20)
Набор для синтеза мРНК in vitro (с ΨTP и m5CTP с ARCA) (ARCA-mRNA-YC-20)
Набор для синтеза мРНК in vitro (с кэпом m7GmAmG) (AG-mRNA- 20)
Набор для синтеза мРНК in vitro (с ARCA) (ARCA-mRNA-20)
4
Очистка мРНК
Очистку синтезированной мРНК можно проводить различными способами: LiCl, фенол-хлороформной экстракции, высокоэффективной жидкостной хроматографии (ВЭЖХ), а также с использованием методов, основанных на спин-колонках. Наиболее удобный и быстрый подход основан на использовании специальных сорбционных колонок. Рекомендуем для рутинных задач использовать набор для очистки из реакционных смесей от компании «Биолабмикс» (DR-250). В случае синтеза коротких РНК рекомендуем использование набора для выделения суммарной и микроРНК из клеток и тканей (LRU-100-50).
Для предотвращения аккумуляции пирофосфата и для повышения выхода РНК в ходе in vitro транскрипции используют фермент пирофосфотазу.
Для удаления примеси ДНК из раствора синтезированной мРНК, необходимо к реакционной смеси добавлять фермент ДНКазу. Обработку ДНКазой можно проводить прямо в транскрипционном буфере непосредственно после реакции. Для достижения наилучших результатов рекомендуем использование термолабильной ДНКазы от компании «Биолабмикс» (EM-100). Термолабильные ДНКазы позволяют проводить инактивацию с помощью нагревания и короткой инкубации при повышенной температуре 55-65°С. Однако, при нагревании нарушается стабильность синтезированных РНК, поэтому мы рекомендуем избегать стадии нагревания и проводить удаление фермента ДНКазы с помощью методов сорбции (например, с использованием наборов DR или RUplus) или ВЭЖХ.
Кроме того, рекомендуем проводить этап удаления фосфатов на 5’-конце, так как некэпированные молекулы РНК с остатками фосфатов являются активными индукторами неспецифического иммунного ответа и способствуют активации процессов деградации РНК в клетках за счет связывания с рядом РНК-рецепторов в клетках.
Проверить качество полученной РНК можно с помощью гель-электрофореза в агарозном геле или с помощью анализа на микрочипах для капиллярного фореза. Для анализа в агарозном геле рекомендуем наносить РНК в Буфере для нанесения на гель «ФриК» (D-3001, Биолабмикс). Количество очищенной мРНК можно оценить с помощью УФ-спектрометрии. Характерный максимум поглощения для РНК: при λ = 260 нм. Для оценки концентрации РНК (мкг/мл) применяется следующая формула: A260 × разбавление × 40 мкг/мл. Характерные соотношения оптической плотности достаточно чистой РНК: A260/A280 ≥ 1.8-2.0, A260/230 ≥ 1.9. Кроме того, рекомендуем использование флуоресцентных методов оценки мРНК, реализованных в приборах Qubit или аналогичных, так как очищенная РНК может содержать примесь невключившихся трифосфатов и фрагментов ДНК-матрицы.
5
Полиаденилирование
Полиаденилирование - важнейший процесс синтеза мРНК, который заключается в присоединении к 3' концу молекулы мРНК последовательности адениновых нуклеотидов, в результате чего формируется так называемый поли(А)-хвост. Эта пост-транскрипционная модификация играет несколько важнейших ролей в созревании и стабильности мРНК. В составе пре-мРНК имеется определенная последовательность нуклеотидов, называемая сигналом полиаденилирования или поли(А) сигналом. У человека эта последовательность обычно имеет вид AAUAAA.
ПолиА-хвост при получении искусственных мРНК можно добавить в виде кодирующей последовательности в составе исходной плазмиды или ПЦР-продукта, а также используя специальный фермент полиА-полимеразу. Ферментативно удается получить максимальную длину полиА, однако такой подход менее технологичен и его сложно масштабировать. Поэтому вариант полиаденилирования нужно подбирать в зависимости от финальной задачи. В каталоге компании Биолабмикс в ближайшее время появится фермент полиА-полимераза, который отлично подходит для решения научных задач по разработке мРНК-вакцин и мРНК-регуляторов.
Kariko K. et al., Immunity, 23, 165-175 (2005).
Karikó K et al., Mol. Ther. 16(11):1833–1840 (2008).
Anderson B.R. et al., NAR, 38 (2010).
Warren L. et al.., Cell Stem Cell, 7, 618-630 (2010).
Karikó K et al., Mol Ther 20(5):948–953 (2012).
Durbin A. F. et al., mBio, 7 (2016)
Stepanov G.A., Zhuravlev E.S. et al. Genes, (2018).
Prokhorova D.V. et al., The CRISPR Journal, 5 (2022).
Hoy A. et al., The CRISPR Journal, 5 (2022).
Таблица комплексного решения
Имя
Каталожный №
Выделений
Цена за шт
Кол-во
Сумма
Имя
Набор Mini для выделения плазмидной ДНК из бактериальных клеток
Выделение плазмидной ДНК из культур клеток E.coli на микроцентрифужных колонках.
Имя
Набор Maxi для выделения плазмидной ДНК из бактериальных клеток
Набор предназначен для выделения и очистки плазмидной ДНК из культур бактериальных клеток E. coli колоночным методом.
Имя
Набор для выделения ДНК и РНК из реакционных смесей
Очистка ДНК и РНК (от 50 до 10000 н.т.) от компонентов реакции, например, от dNTP, ферментов, не
включившихся низкомолекулярных радиоактивных и флуоресцентных меток и др. на микроцентрифужных колонках.
Имя
Набор для выделения РНК на колонках (модифицированный)
Набор для выделения РНК из культур эукариотических клеток, культур клеток грамотрицательных и грамположительных бактерий, мазков или соскобов эпителиальных клеток, вирусов.
В процессе выделения целостность РНК сохраняется. Возможно выделение до 50 мкг РНК.
Имя
Набор для выделения РНК суммарной и микроРНК из клеток и тканей
Выделение и очистка суммарной РНК и малых форм РНК (до 200 н.т., включая микроРНК) из культур клеток животных и бактерий, тканей животных и растений.
Имя
Каталожный №
Количество мкл
Цена за шт
Кол-во
Сумма
Имя
Набор 100 мМ растворов ATP, GTP, CTP, UTP (rNS-1** в воде, rNS-4** в TE буфере)
Набор из 4х пробирок, содержащих по отдельности стерильные 100 мМ растворы ATP, GTP, CTP и UTP в виде аммонийных солей в воде (rNS-101, rNS-110) или в ТЕ буфере (rNS-401, rNS-410). Чистота каждого из нуклеодидов ≥ 98% (HPLC).
Имя
Набор для проведения ПЦР с Фьюжн ДНК-полимеразой
Набор реагентов для постановки ПЦР с высокоточной Фьюжн ДНК-полимеразой. В набор входят отдельные компоненты такие как ионы магния, смесь дезоксинуклеотидтрифосфатов (dNTP) и диметилсульфоксид.
Имя
N6-метиладенозин-5`-трифосфат
Стерильный 100 мМ раствор N6-метиладенозин-5`-трифосфата в виде аммонийной соли в воде. Чистота нуклеотида ≥ 96% (HPLC).
Имя
Аналог кэпа m7GmAmG
Стерильный 100 мМ раствор аналога кэпа m7G(3`OMe)pppA(2`OMe)pG в виде аммонийной соли в воде. Аналог CleanCap AG (3' OMe)
Имя
5-метилцитидин-5`-трифосфат
Стерильный 100 мМ раствор 5-Me-СTP в виде натриевой соли в воде. Чистота нуклеотида ≥ 96% (HPLC).
Имя
Псевдоуридин-5`-трифосфат
Стерильный 100 мМ раствор Pseudo-UTP в виде натриевой соли в воде. Чистота нуклеотида ≥ 96% (HPLC).
Имя
N1-метил-псевдоуридин-5`-трифосфат
Стерильный 100 мМ раствор N1-Me-PseudoUTP в виде натриевой соли в воде. Чистота нуклеотида ≥ 96% (HPLC).
Имя
Аналог структуры кэпа ARCA
Стерильный 100 мМ раствор аналога структуры кэпа ARCA в виде аммонийной соли в воде. Чистота нуклеотида ≥ 96% (HPLC).
Имя
Каталожный №
Количество, е.а.
Цена за шт
Кол-во
Сумма
Имя
ДНК-зависимая РНК-полимераза Т7
Высокопроцессивная ДНК-зависимая РНК-полимераза из бактериофага Т7 (T7 РНК-полимераза, РНК-полимераза фага T7), специфично взаимодействующая с Т7-промотором и катализирующая синтез фрагментов РНК в направлении 5`->3` на ДНК-матрице.
Имя
Ингибитор РНКаз
Ингибитор РНКаз представляет собой рекомбинантный белок массой 50 кДа, экспрессируемый в E.coli. Он ингибирует рибонуклеазную активность эукариотических ферментов, таких как РНКаза A, РНКаза B, РНКаза C, и защищает РНК от неспецифического гидролиза.
Ингибитор РНКаз предназначен для использования в приложениях, где присутствие РНКаз может снизить качество результатов экспериментов, например при выделении РНК, синтезе кДНК, ОТ-ПЦР, транскрипции и трансляции in vitro.
Имя
Каталожный №
Количество реакций (50 мкл)
Цена за шт
Кол-во
Сумма
Имя
Набор для синтеза мРНК in vitro (с m7GmAmG)
Набор предназначен для постановки реакции транскрипции in vitro для получения m7G-кэпированной мРНК. В состав набора входит аналог CleanCap AG (3' OMe)
Имя
Набор для синтеза мРНК in vitro (с ARCA)
Набор предназначен для постановки реакции транскрипции in vitro для получения ARCA-кэпированной мРНК.
Имя
Набор для синтеза мРНК in vitro (с ΨTP и m5CTP с m7GmAmG)
Набор предназначен для постановки реакции транскрипции in vitro для получения m7G-кэпированной мРНК, содержащей в структуре модифицированные нуклеотиды: псевдоуридин (Ψ), 5-метилцитидин (m5C). В состав набора входит аналог CleanCap AG (3' OMe)
Имя
Набор для синтеза мРНК in vitro (с ΨTP и m5CTP с ARCA)
Набор для синтеза мРНК in vitro (с ΨTP и m5CTP с ARCA) предназначен для постановки реакции транскрипции in vitro для получения ARCA-кэпированной мРНК, содержащей в структуре модифицированные нуклеотиды: псевдоуридин (Ψ), 5-метилцитидин (m5C). Полученная в результате транскрипции мРНК может быть использована для изучения функций мРНК, для микроинъекций, для трансфекции клеток, для трансляции in vitro и др.
Имя
Набор для синтеза мРНК in vitro
Набор для синтеза мРНК in vitro предназначен для постановки реакции транскрипции in vitro для получения мРНК. Полученная в результате транскрипции мРНК может быть использована для изучения функций мРНК, для микроинъекций, для трансфекции клеток, для трансляции in vitro и др.
Имя
Набор для проведения T7-транскрипции in vitro
Принцип действия набора основан на ферментативном синтезе молекул РНК на ДНК-матрице при помощи ДНК-зависимой РНК-полимеразы бактериофага T7. В состав набора входят все необходимые реагенты для получения высокого выхода РНК-транскриптов за минимальное время реакции.
Полученная РНК может быть использована для изучения структуры и функций РНК, для систем геномного редактирования в качестве направляющей РНК, для исследования механизмов РНК-интерференции, для трансфекции клеток, для трансляции in vitro и др.
Имя
Каталожный №
Количество мл
Цена за шт
Кол-во
Сумма
Имя
Стерильная вода
Стерильная вода, обработанная диэтилпирокарбонатом (ДЭПК), свободная от РНКаз и ДНКаз, с удельным сопротивлением 16-18 МОм*см, предназначена для работы c нуклеиновыми кислотами.
Имя
Буфер для нанесения образцов РНК на гель «ФриК»
Содержит формамид и бромистый этидий для эффективной денатурации и окрашивания РНК. Содержит два красителя для оценки подвижности в геле: бромфеноловый синий и ксиленцианол FF.
